
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Hem B | |
 | |
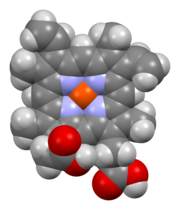 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C34H32O4N4Fe |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 616,487 g/mol |
| Ďalšie informácie | |
| Číslo CAS | 14875-96-8 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Hem B je najbežnejší druh hemu.[1] Nachádza sa napríklad v hemoglobíne a myoglobíne, čo sú bielkoviny, ktoré prenášajú kyslík. Enzýmová rodina peroxidáz takisto obsahuje hem B. Cyklooxygenázy COX-1 a COX-2 takisto obsahujú hem B na jednom zo svojich dvoch aktívnych miest.
Štruktúra
Hem B je štruktúrne najmenší zo základných hemov. Na uhlíkoch 3 a 8 obsahuje vinylovú skupinu a na uhlíku 18 má metylovú skupinu.[2]
Štruktúru hemu B a hemu S ako prvý určil nemecký chemik Hans Fischer.[3]
Väzba
Hem b sa na bielkovinu viaže nekovalentne.[1][2] Všeobecne je hem B naviazaný na bielkovinu (apoproteín bez koenzýmu) pomocou jednej koordinačnej väzby medzi iónom železa a bočným reťazcom aminokyseliny. Najčastejšie je touto aminokyselinou histidín, okrem neho sa však v axiálnej polohe vyskytuje aj cysteín, metionín, tyrozín a lyzín.[2] V hemoglobíne i myoglobíne tvorí túto koordinačnú väzbu evolučne zachovaný histidín. Syntáza oxidu dusnatého a cytochróm P450, ktoré takisto obsahujú hem B, majú evolučne zachovaný cysteín.
Keďze ión železa je v bielkovinách obsahujúcich hem B viazaný na štyri atómy dusíka porfyrínu (ktoré sú v rovine) a jeden atóm proteínu (z bočného reťazca aminokysliny), tento ión sa často nachádza v pentakoordinovanom stave (tvorí päť väzieb). Pri naviazaní kyslíku alebo toxického oxidu uhoľnatého sa železo dostáva do hexakoordinovaného stavu.
Referencie
- ↑ a b BOWMAN, Sarah E. J.; BREN, Kara L.. The chemistry and biochemistry of heme c: functional bases for covalent attachment. Natural Product Reports, 2008, roč. 25, čís. 6, s. 1118. Dostupné online . ISSN 0265-0568. DOI: 10.1039/b717196j. (po anglicky)
- ↑ a b c LI, Ting; BONKOVSKY, Herbert L; GUO, Jun-tao. Structural analysis of heme proteins: implications for design and prediction. BMC Structural Biology, 2011-12, roč. 11, čís. 1, s. 13. Dostupné online . ISSN 1472-6807. DOI: 10.1186/1472-6807-11-13. (po anglicky)
- ↑ FISCHER, H.; ORTH, H.. Die Chemie des Pyrrols. Liepzig : Akademische Verlagsgesellschaft, 1934.
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Heme B na anglickej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk
