
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
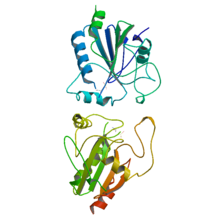
Peroxidázy alebo peroxidreduktázy (EC 1.11.1.-) tvoria veľkú skupinu enzýmov, ktoré majú dôležité úlohy v rôznych biologických procesoch. Sú pomenované podľa svojej schopnosti rozkladať (redukovať) peroxidy.[1] Peroxidázy majú predovšetkým obrannú úlohu alebo sa účastnia biosyntézy (napr. bunkovej steny u rastlín alebo hormónu tyroxínu).[2] Medzi peroxidázy patrí aj kataláza, ktorá je však schopná peroxid vodíka i oxidovať.[1]
Funkcia
Peroxidázy typicky katalyzujú nasledovnú reakciu:[3]
Peroxidázy teda v procese rozkladu peroxidu vodíka oxidujú nejaký substrát.[2] V prípade katalázy je donor elektrónov druhá molekula peroxidu vodíka.[3]
Substrát, aktívne miesto, donor elektrónov
Pre mnohé peroxidázy je optimálnym substrátom peroxid vodíka, ale niektoré majú vyššiu aktivitu pri rozklade organických hydroperoxidov, napríklad lipoperoxidov.[3]
Peroxidázy môžu v aktívnom mieste obsahovať hemový kofaktor alebo majú redoxne aktívne cysteínové či selenocysteínové reziduum. Niektoré peroxidázy majú namiesto toho v aktívnom mieste vanád alebo mangán.[3]
Ako donor elektrónov môžu fungovať rôzne látky.[4] Napríklad:
- Chrenová peroxidáza môže použiť mnoho rôznych organických zlúčenín ako donory a akceptory elektrónov. Tento enzým má dobre dostupné aktívne miesto, ktoré je prístupné mnohým zlúčeninám.[chýba zdroj
- Naproti tomu iné enzýmy, napríklad cytochróm c peroxidáza, majú úzke aktívne miesto, takže sú schopné využiť len málo látok ako donory elektrónov.[chýba zdroj
U mnohých týchto enzýmov úplne chýba väzbové miesto pre oxidovaný substrát. Dokonca i krátke peptidy (8-12 aminokyselín) kovalentne naviazané na hem, ktoré obsahujú histidín ako proximálny ligand pre hem, vykazujú peroxidázovú aktivitu.[2]
Klasifikácia
Medzi rodiny peroxidáz patria:[5]
- hemové peroxidázy
- hlavné superrodiny:
- (neživočíšne) hemové peroxidázy (rastlinné, bakteriálne, hubové) - hem sa viaže nekovalentne, ďalej sa delia na tri rodiny[3]
- živočíšne hem-dependentné peroxidázy - hem je kovalentne viazaný[3]
- Dy-P rodina peroxidáz
- katalázy
- niektoré haloperoxidázy
- dihemová cytochróm c peroxidáza
- hlavné superrodiny:
- nehemové peroxidázy
- tiolové (a selenolové):[3]
- niektoré haloperoxidázy
- alkylhydroperoxidreduktáza
- mangánová peroxidáza
- NADH peroxidáza
Charakterizácia
Glutatiónperoxidázová rodina sa skladá z 8 známych ľudských izoforiem. Glutatiónperoxidáza využíva glutatión ako donor elektrónov a je schopná pôsobiť na peroxid vodíka i organické hydroperoxidy. Bolo ukázané, že Gpx1,Gpx2, Gpx3 a Gpx4 sú enzýmy obsahujúce selén, zatiaľ čo Gpx6 je u ľudí selenoproteín a u hlodavcov sa nachádza ako homológ bohatý na cysteín. Gpx5 neobsahuje selenocysteín, ale cysteín.[3]
Amyloid beta po naviazaní na hem takisto vykazuje peroxidázovú aktivitu.[6]
Typickou skupinou peroxidáz sú haloperoxidázy. Táto skupina je schopná reagovať s halogenidmi[3] a i prírodnými organohalogenidmi.[chýba zdroj
Väčšinu aminokyselinových sekvencií peroxidáz je možné nájsť v databáze PeroxiBase.
Rezistencia na patogény
Aj keď presný mechanizmus zatiaľ nie je známy, peroxidázy majú úlohu v posilňovaní obranyschopnosti rastlín voči patogénom.[7] Mnohé druhy Solanaceae, hlavne Solanum melongena (baklažán) a Capsicum chinense (paprika čínska), používajú guajakol a enzým guajakolperoxidázu na obranu voči bakteriálnym parazitom, ako je napríklad Ralstonia solanacearum – expresia génu tohto enzýmu začína už minúty po napadnutí baktériou.[8]
Použitie
Peroxidázy možno použiť na čistenie odpadových vôd. Je tak možné odstrániť napríklad fenoly, ktoré patria medzi významné polutanty, pomocou enzýmom katalyzovanej polymerizácie za použitia chrenovej peroxidázy[9] alebo peroxidázy zo zemiakov[10] či iných.[11] Fenoly sa oxidujú na fenoxy radikály, ktoré potom reagujú za vzniku oligomérov a polymérov, ktoré sú menej toxické než samotné fenoly. Takisto je možné použiť peroxidázy na premenu toxických látok na menej škodlivé látky.
Prebieha i výskum použitia peroxidáz v rôznych výrobných procesoch, napríklad na výrobu adhezív, počítačových čipov, súčiastok na výrobu áut a obloženie bubna či plechoviek. Iné štúdie ukázali, že peroxidázy možno použiť na polymerizáciu anilínov a fenolov v organických rozpúšťadlách.[12]
Použitie peroxidáz na asymetrickú syntézu chirálnych sulfoxidov bolo takisto preskúmané.[13]
Peroxidázy sa niekedy používajú ako histologické markery.[chýba zdroj
Referencie
- ↑ a b kataláza. In: Encyclopaedia Beliana. 1. vyd. Bratislava : Encyklopedický ústav SAV; Veda, © 1999.
- ↑ a b c EVERSE, Johannes. Heme Proteins. New York : Elsevier, 2004-01-01. DOI: 10.1016/B0-12-443710-9/00304-5. Dostupné online. ISBN 978-0-12-443710-4. DOI:10.1016/b0-12-443710-9/00304-5 S. 354–361. (po anglicky)
- ↑ a b c d e f g h i BINDOLI, A.; RIGOBELLO, M. P.. Peroxidase Biochemistry and Redox Signaling. Waltham : Academic Press, 2013-01-01. DOI: 10.1016/B978-0-12-378630-2.00179-1. Dostupné online. ISBN 978-0-12-378631-9. DOI:10.1016/b978-0-12-378630-2.00179-1 S. 407–412. (po anglicky)
- ↑ NICOLAS, J.; BILLAUD, C.; PHILIPPON (RETIRED), J.. BROWNING | Enzymatic – Biochemical Aspects. Oxford : Academic Press, 2003-01-01. DOI: 10.1016/B0-12-227055-X/00129-2. Dostupné online. ISBN 978-0-12-227055-0. DOI:10.1016/b0-12-227055-x/00129-2 S. 678–686. (po anglicky)
- ↑ RedOxiBase: Peroxidase Classes . . Dostupné online. Archivované 2019-11-22 z originálu.
- ↑ Amyloid-beta peptide binds with heme to form a peroxidase: relationship to the cytopathologies of Alzheimer's disease. Proceedings of the National Academy of Sciences of the United States of America, Feb 2006, s. 3381–6. DOI: 10.1073/pnas.0600134103. PMID 16492752.
- ↑ Induction of resistance in host against the infection of leaf blight pathogen (Alternaria palandui) in onion (Allium cepa var aggregatum). Indian Journal of Biochemistry & Biophysics, Dec 2005, s. 371–7. PMID 16955738.
- ↑ Prakasha, A, Umesha, S. Biochemical and Molecular Variations of Guaiacol Peroxidase and Total Phenols in Bacterial Wilt Pathogenesis of Solanum melongena. Biochemistry & Analytical Biochemistry, 5,292, 2016
- ↑ COOPER, V.A.; NICELL, J.A.. Removal of phenols from a foundry wastewater using horseradish peroxidase. Water Research, 1996-04, roč. 30, čís. 4, s. 954–964. Dostupné online . DOI: 10.1016/0043-1354(95)00237-5. (po anglicky)
- ↑ KURNIK, Katarzyna; TREDER, Krzysztof; SKORUPA-KŁAPUT, Monika. Removal of Phenol from Synthetic and Industrial Wastewater by Potato Pulp Peroxidases. Water, Air, & Soil Pollution, 2015-08, roč. 226, čís. 8, s. 254. Dostupné online . ISSN 0049-6979. DOI: 10.1007/s11270-015-2517-0. (po anglicky)
- ↑ SINGH, Savita; MISHRA, Ruchi; SHARMA, Radhey Shyam. Phenol remediation by peroxidase from an invasive mesquite: Turning an environmental wound into wisdom. Journal of Hazardous Materials, 2017-07, roč. 334, s. 201–211. Dostupné online . DOI: 10.1016/j.jhazmat.2017.04.007. (po anglicky)
- ↑ Tuhela, L., G. K. Sims, and O. Tuovinen. 1989. Polymerization of substituted anilines, phenols, and heterocyclic compounds by peroxidase in organic solvents. Columbus, Ohio: The Ohio State University. 58 pages.
- ↑ GROGAN, G.. 7.14 Oxidation: Asymmetric Enzymatic Sulfoxidation. Amsterdam : Elsevier, 2012-01-01. DOI: 10.1016/B978-0-08-095167-6.00718-7. Dostupné online. ISBN 978-0-08-095168-3. DOI:10.1016/b978-0-08-095167-6.00718-7 S. 295–328. (po anglicky)
Pozri aj
- Askorbátperoxidáza
- Chloridperoxidáza
- Cytochróm c peroxidáza
- Haloperoxidáza
- Hemoproteín
- Imunoperoxidáza
- Laktoperoxidáza
- Myeloperoxidáza
- Tyroidperoxidáza
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Peroxidase na anglickej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk

