
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Hexanol | |
|---|---|
| Systematický název | hexan-1-ol |
| Ostatní názvy | hexanol |
| Funkční vzorec | CH3(CH2)5OH |
| Sumární vzorec | C6H14O |
| Vzhled | bezbarvá kapalina (všechny izomery) |
| Identifikace | |
| Registrační číslo CAS | 111-27-3 |
| EC-no (EINECS/ELINCS/NLP) | 203-852-3 |
| PubChem | 8103 |
| SMILES | CCCCCCO |
| InChI | 1S/C6H14O/c1-2-3-4-5-6-7/h7H,2-6H2,1H3 |
| Číslo RTECS | MQ4025000 |
| Vlastnosti | |
| Molární hmotnost | 102,104 465 070 g/mol |
| Teplota tání | −53 až −41 °C (1-hexanol) |
| Teplota varu | 119 až 159 °C (podle izomeru), 155 až 159 °C (1-hexanol) |
| Hustota | 0,831 6 g/cm3 (1-hexanol) |
| Rozpustnost ve vodě | 0,59 g/100 ml (20 °C) |
| Rozpustnost v polárních rozpouštědlech | mísitelný s ethanolem a etherem |
| Bezpečnost | |
| [1] Varování[1] | |
| H-věty | H302 |
| R-věty | R22 |
| S-věty | S2, S24/25 |
| NFPA 704 |  2
1
0
|
| Teplota vzplanutí | 59 °C (1-hexanol) |
| Teplota vznícení | 293 °C (1-hexanol) |
Některá data mohou pocházet z datové položky. | |
Hexanol (CH3(CH2)5OH, sumární vzorec C6H14O) je organická sloučenina, alkohol, šestý člen homologické řady alkanolů (alkoholů odvozených od alkanů).
Hexanol má celkem 17 izomerů:
| Struktura | Typ | Systematický název | Teplota varu (°C) |
|---|---|---|---|
| primární | hexan-1-ol | 158 | |
|
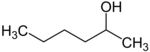
sekundární | hexan-2-ol | 136 |
| sekundární | hexan-3-ol | 135 | |
|
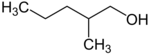
primární | 2-methylpentan-1-ol | 147 |

|
primární | 3-methylpentan-1-ol | 152 |
|
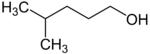
primární | 4-methylpentan-1-ol | 151 |

|
terciární | 2-methylpentan-2-ol | 121 |

|
sekundární | 3-methylpentan-2-ol | 134 |
|
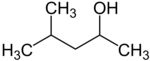
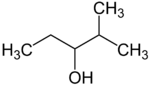
sekundární | 4-methylpentan-2-ol | 131 |
|
sekundární | 2-methylpentan-3-ol | 126 |

|
terciární | 3-methylpentan-3-ol | 122 |

|
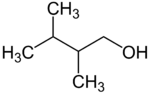
primární | 2,2-dimethylbutan-1-ol | 137 |
|
primární | 2,3-dimethylbutan-1-ol | 145 |

|
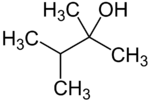
primární | 3,3-dimethylbutan-1-ol | 143 |
|
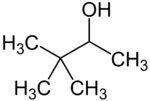
terciární | 2,3-dimethylbutan-2-ol | 119 |
|
sekundární | 3,3-dimethylbutan-2-ol | 120 |

|
primární | 2-ethylbutan-1-ol | 146 |
Příprava
Průmyslově se hexanol vyrábí oligomerizací ethylenu za použití triethylhliníku[2]:
Al(C2H5)3 + 6 C2H4 → Al(C6H13)3
2 Al(C6H13)3 + 3 O2 + 6 H2O → 6 HOC6H13 + Al(OH)3.
Tento proces vytváří mnoho oligomerů, které se dají oddělit destilací.
Alternativní metody
Další metodou přípravy hexanolu má za následek hydroformylaci pentenu následovanou hydrogenací aldehydů. Tato metoda je používána v průmyslu k výrobě směsi izomerů, které jsou prekurzory plastifikátorů.
Hexen může být převeden na hexanol (Katalyzátory jsou diboran v tetrahydrofuranu, peroxid vodíku a hydroxid sodný):
Tato metoda se používá v laboratorní syntéze, ovšem nikoliv v praxi.
Reference
V tomto článku byl použit překlad textu z článku 1-Hexanol na anglické Wikipedii.
- ↑ a b 1-Hexanol. pubchem.ncbi.nlm.nih.gov . PubChem . Dostupné online. (anglicky)
- ↑ FALBE, Jürgen; BAHRMANN, Helmut; LIPPS, Wolfgang; MAYER, Dieter. Alcohols, Aliphatic. : DOI 10.1002/14356007.a01_279.
Externí odkazy
 Obrázky, zvuky či videa k tématu Hexanol na Wikimedia Commons
Obrázky, zvuky či videa k tématu Hexanol na Wikimedia Commons
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk



