A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Prolín | ||||||||||||||||||||
| Všeobecné vlastnosti | ||||||||||||||||||||
| Sumárny vzorec | C5H9NO2 | |||||||||||||||||||
| Fyzikálne vlastnosti | ||||||||||||||||||||
| Molekulová hmotnosť | 115,1 u | |||||||||||||||||||
| Molárna hmotnosť | 115,13 g/mol | |||||||||||||||||||
| Teplota rozkladu | 205-228 °C | |||||||||||||||||||
| Hustota | 1,35 – 1,38 g/cm³ (25 °C) | |||||||||||||||||||
| ||||||||||||||||||||
| Ďalšie informácie | ||||||||||||||||||||
| Číslo CAS | 147-85-3 (L-prolín) 344-25-2 (D-prolín) 609-36-9 (racemát) | |||||||||||||||||||
| EINECS číslo | 205-702-2 | |||||||||||||||||||
| Číslo RTECS | TW3584000 | |||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | ||||||||||||||||||||
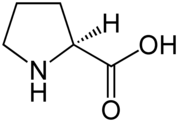
Prolín (skratka Pro alebo P[1]) je jedna zo základných dvadsiatich proteínogénnych aminokyselín, ktorá vo svojej štruktúre neobsahuje primárnu aminoskupinu (NH2), ale sekundárnu (NH). Prolín sa radí medzi nepolárne aminokyseliny a nepatrí medzi esenciálne aminokyseliny.
Prolín je nezlučiteľný s niektorými sekundárnymi štruktúrami proteínov (α-helix, β-list), zato sa veľmi často vyskytuje v β-otáčkach.[2] Dôvodom je rigidita jeho bočného reťazca a práve jeho sekundárna aminoskupina, ktorá v peptidovej väzbe stabilizuje cis-konfiguráciu (na rozdiel od bežnejšej a stabilnejšej trans-konfigurácie). Cis-konfigurácia mení smer peptidového reťazca (preto narušuje štruktúru α-helixu i β-listu) a naopak stabilizuje β-otáčku. Niektoré bielkoviny vo svojej štruktúre vyžadujú prítomnosť cis-konfiguráciu peptidovej väzby u aminokyseliny pred prolínom na niektorých pozíciách v sekvencii. Cis-trans izomerizáciu tejto peptidovej väzby katalyzujú prolylizomerázy.
Deriváty
Medzi významné deriváty prolínu patrí 4-hydroxyprolín, ktorý vzniká postranslačnou hydroxyláciou prolínu v kolagéne.[3]
Referencie
- ↑ Nomenclature and Symbolism for Amino Acids and Peptides . iupac.qmul.ac.uk, . Dostupné online.
- ↑ IMAI, Kenichiro; MITAKU, Shigeki. Mechanisms of secondary structure breakers in soluble proteins. BIOPHYSICS, 2005, roč. 1, s. 55–65. Dostupné online . ISSN 1349-2942. DOI: 10.2142/biophysics.1.55. (po anglicky)
- ↑ SZPAK, Paul. Fish bone chemistry and ultrastructure: implications for taphonomy and stable isotope analysis. Journal of Archaeological Science, 2011-12-01, roč. 38, čís. 12, s. 3358–3372. Dostupné online . ISSN 0305-4403. DOI: 10.1016/j.jas.2011.07.022. (po anglicky)
Iné projekty
 Commons ponúka multimediálne súbory na tému Prolín
Commons ponúka multimediálne súbory na tému Prolín
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Prolin na českej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk