
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Chlorid yttritý | |
|---|---|
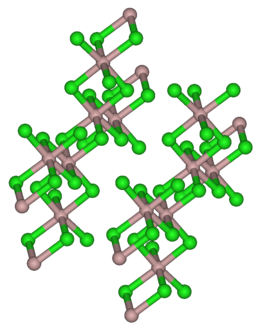 Struktura krystalů chloridu yttritého, podobná struktuře chloridu hlinitého | |
| Obecné | |
| Systematický název | Chlorid yttritý |
| Anglický název | Yttrium(III) chloride Yttrium trichloride |
| Německý název | Yttrium(III)-chlorid |
| Sumární vzorec | YCl3 |
| Vzhled | bílá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 10361-92-9 |
| SMILES | Cl(Cl)Cl |
| InChI | 1S/3ClH.Y/h3*1H;/q;;;+3/p-3 1/3ClH.Y/h3*1H;/q;;;+3/p-3 |
| Číslo RTECS | ZG3150000 |
| Vlastnosti | |
| Molární hmotnost | 195,26 g/mol |
| Teplota tání | 721 °C |
| Teplota varu | 1 507 °C |
| Hustota | 2,67 g/cm3 |
| Rozpustnost ve vodě | 82 g/100 ml |
| Rozpustnost v polárních rozpouštědlech | ethanol 60,1 g/100 ml (15 °C) |
| Rozpustnost v nepolárních rozpouštědlech | pyridin 60,6 g/100 ml (15 °C) |
| Struktura | |
| Krystalová struktura | jednoklonná |
| Bezpečnost | |
| Teplota vznícení | nehořlavý |
Některá data mohou pocházet z datové položky. | |
Chlorid yttritý (YCl3) je sloučenina yttria a chloru. Jedná se o pevnou látku, která je dobře rozpustná jak v polárních (voda, ethanol), tak i v nepolárních (pyridin...) rozpouštědlech
Vlastnosti
Chlorid yttritý existuje ve dvou formách, bezvodý YCl3 a také jako hexahydrát YCl3·6 H2O, obě formy jsou bílé pevné a dobře rozpustné látky. Jeho krystalická struktura je podobná struktuře mnoha sloučenin jako například AlCl3.
Příprava
YCl3 se připravuje z Y2O3[1][2] nebo YCl3·6 H2O[3] a chloridu amonného, přičemž u obou postupů vzniká jako komplexní meziprodukt (NH4)2:
10 NH4Cl + Y2O3 → 2 (NH4)2 + 6 NH3 + 3 H2O
YCl3·6H2O + 2 NH4Cl → (NH4)2 + 6 H2O
Meziprodukt se následně rozloží zahřátím podle rovnice:
(NH4)2 → 2 NH4Cl + YCl3
Reakcí oxidu yttritého s HCl vzniká hexahydrát, ze kterého nelze připravit bezvodý YCl3 zahřátím, místo toho vzniká oxychlorid.
Podobné sloučeniny
Reference
V tomto článku byl použit překlad textu z článku Yttrium(III) chloride na anglické Wikipedii.
- ↑ MEYER, G. The Ammonium Chloride Route to Anhydrous Rare Earth Chlorides-The Example of YCl3. Inorganic Syntheses. 1989, s. 146–150. ISBN 978-0-470-13256-2. DOI 10.1002/9780470132562.ch35.
- ↑ EDELMANN, F. T.; POREMBA, P. Synthetic Methods of Organometallic and Inorganic Chemistry. Redakce Herrmann, W. A. (ed.). Stuttgart: Georg Thieme Verlag, 1997. ISBN 3-13-103021-6.
- ↑ TAYLOR, M.D.; CARTER, C.P. Preparation of anhydrous lanthanide halides, especially iodides. Journal of Inorganic and Nuclear Chemistry. S. 387–391. DOI 10.1016/0022-1902(62)80034-7.
Externí odkazy
 Obrázky, zvuky či videa k tématu chlorid yttritý na Wikimedia Commons
Obrázky, zvuky či videa k tématu chlorid yttritý na Wikimedia Commons
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk
