A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Chlorid dusitý | ||||||||||||||||||||||||
| Všeobecné vlastnosti | ||||||||||||||||||||||||
| Sumárny vzorec | NCl3 | |||||||||||||||||||||||
| Synonymá | trichlóramín trichlórnitrid chlorodusík | |||||||||||||||||||||||
| Vzhľad | žltá olejovitá kvapalina | |||||||||||||||||||||||
| Fyzikálne vlastnosti | ||||||||||||||||||||||||
| Molekulová hmotnosť | 120,4 u | |||||||||||||||||||||||
| Molárna hmotnosť | 120,365 g/mol | |||||||||||||||||||||||
| Teplota topenia | −40 °C | |||||||||||||||||||||||
| Teplota varu | 71 °C | |||||||||||||||||||||||
| Hustota | 1,635 g/cm³ | |||||||||||||||||||||||
| Rozpustnosť | vo vode: takmer nerozpustný (pomalá hydrolýza) | |||||||||||||||||||||||
| Termochemické vlastnosti | ||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | +232 kJ/mol | |||||||||||||||||||||||
| ||||||||||||||||||||||||
| Ďalšie informácie | ||||||||||||||||||||||||
| Číslo CAS | 10025-85-1 | |||||||||||||||||||||||
| EINECS číslo | 233-045-1 | |||||||||||||||||||||||
| Číslo RTECS | QW974000 | |||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | ||||||||||||||||||||||||
Chlorid dusitý (NCl3, iné názvy: trichlóramín, trichlórnitrid, chlorodusík) je anorganická zlúčenina. Táto žltá, olejovitá, štipľavo páchnuca kvapalina je najrozšírenejším vedľajším produktom reakcií medzi derivátmi amoniaku a chlórom (napríklad v plaveckých bazénoch pri reakcii moču plavcov s chlórom, ktorý sa do vody pridáva kvôli dezinfekcii).
V čistej forme je chlorid dusitý vysoko reaktívny. V malých množstvách môže vznikať pri dezinfekcii pitnej vody monochlóramínom, vyššie hladiny môžu dráždiť sliznice.[1] Chlorid dusitý vyrábaný pod obchodnou značkou Agen sa používal na bielenie a dozrievanie múky. Má rovnaký účinok ako slzný plyn, ale nikdy nebol na tento účel používaný.[2]
Príprava a štruktúra
Zlúčenina sa pripravuje pôsobením chlóru na amónne soli, ako napríklad dusičnan amónny:
- 4 NH3 + 3 Cl2 → NCl3 + 3 NH4Cl
Medziprodukty v tejto konverzii sú chlóramín a dichlóramín (NH2Cl, resp. NHCl2).
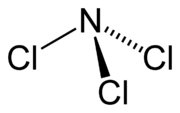
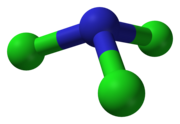
Podobne ako amoniak, aj chlorid dusitý má pyramídovú molekulu.
Reakcia
Oxidačné číslo dusíka v chloride dusitom sa často uvažuje ako +3, atómy chlóru potom majú oxidačné číslo −1. Väčšina reaktívnych vlastností je s týmto popisom konzistentné.
Chlorid dusitý sa v horúcej vode hydrolyzuje na amoniak a kyselinu chlórnu: NCl3 + 3 H2O → NH3 + 3 HClO
Bezpečnosť
Chlorid dusitý je nebezpečná výbušnina. Je citlivý na svetlo, teplo a prítomnosť organických zlúčenín. Pierre Louis Dulong ho prvýkrát pripravil v roku 1812, pri dvoch explóziách prišiel o dva prsty a oko. Následkom výbuchu chloridu dusitého bol dočasne oslepený Sir Humphry Davy, ktorý preto zamestnal ako svojho spolupracovníka Michaela Faradaya. Belgickí vedci ohlásili možné spojenie medzi chloridom dusitým a vzostupom počtu prípadov astmy u detí, čo nazvali hypotézou bazénového chlóru. [3]
Podobné látky
- Bromid dusitý
- Fluorid dusitý
- Jodid dusitý
- Chlorid arzenitý
- Chlorid fosforitý
- Monochlóramín
- Dichlóramín
- Oxychlorid dusný
Referencie
- ↑ National Institute for Occupational Safety and Health. (2008, August). NIOSH eNews , 6 (4). Retrieved August 27, 2008, from http://www.cdc.gov/niosh/enews/enewsV6N4.html
- ↑ George Clifford White: The handbook of chlorination and alternative disinfectants. 4th Edition, Wiley, 1999, ISBN 978-0-471-29207-4, p 322
- ↑ Bernard A, Carbonnelle S, de Burbure C, Michel O, Nickmilder M. Chlorinated pool Attendance, Atop, and the risk of asthma during childhood. Environmental Health Perspectives , 2006, roč.114, čís. 10, s 1567-1573. Dostupné online. DOI:10.1289/ehp.8461. PMID 17035144
Literatúra
- Janderu, J. (1976). Adv. Inorg. Chem. Radiochem. 19:2.
- P. Kovacic; M. K. Lowery; K. W. Field. Chemistry of N-bromamines and N-chloramines. Chemical Reviews, 1970, roč. 70, čís. 6, s. 639. DOI: 10.1021/cr60268a002.
- Hartl, H.; Schoner, J.; Jander, J.; Schulz, H. Structure of Solide Nitrogen-Trichloride (-125 °C). Zeitschrift für Anorganische und Allgemeine Chemie, 1975, roč. 413, čís. 1, s. 61–71. DOI: 10.1002/zaac.19754130108.
- Cazzoli, G.; Favero, P. G.; Dalborgo, A.. Molecular-Structure, Nuclear-Quadruple Coupling-Constant and Dipole-Moment of Nitrogen Trichloride from Microwave Spectroscopy. Journal of Molecular Spectroscopy, 1974, roč. 50, čís. 1-3, s. 82. DOI: 10.1016/0022-2852(74)90219-7.
- Bayersdo, L.; Engelhar, U.; Fischer, J.; Hohne, K.; Jander, J. Nitrogen-chlorine compounds: Infrared spectra and Raman spectra of nitrogen trichloride. Zeitschrift für anorganische und allgemeine Chemie, 1969, roč. 366, čís. 3-4, s. 169-. DOI: 10.1002/zaac.19693660308.
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Chlorid dusitý na českej Wikipédii.
Externé odkazy
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk