A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
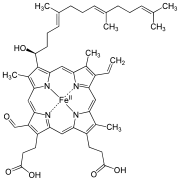
| Hem A | |
 | |
 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C49H56O6N4Fe |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 852,837 g/mol |
| Ďalšie informácie | |
| Číslo CAS | 18535-39-2 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Hem A je druh hemu, čo je koordinačný komplex pozostávajúci z makrocyklického ligandu, patriaceho medzi porfyrín, ktorý cheluje atóm železa. Hem A je biomolekula, ktorá je prirodzene produkovaná mnohými organizmami. V roztoku má dichroicku zeleno-červenú farbu. Štruktúrne je podobný hemu B, ktorý je súčasťou hemoglobínu, červeného farbiva v krvi.
Vzťah k ostatným hemom
Hem A sa líši od hemu B v tom, že metylová skupina na uhlíku 8 v kruhu je oxidovaná na formylovú skupinu a na vinylovú skupinu na uhlíku 2 je naviazaná hydroxyfarnezylová skupina, ktorá patrí medzi izoprenoidy. Hem A sa podobá na hem O, keďže obe majú farnezylovú skupinu na uhlíku 2, ale hem O nemá formylovú skupinu na uhlíku 8, namiesto ktorej má metylovú skupinu. Správna štruktúra hemu A, určená pomocou meraní NMR a IR spektroskopií, zistená pre redukované podobnu komplexu (s FeII), bola prvýkrát publikovaná v roku 1975.[1] Štruktúra bola potom potvrdená syntézou dimetylesteru hemu A bez atómu železa.[2]
História
Hem A ako prvý izoloval nemecký biochemik Otto Warburg v roku 1951. Warburg takisto ukázal, že je to aktívna zložka integrálneho membránového metaloproteínu cytochróm c oxidázy.[3]
Stereochémia
Poslednou otázkou v štruktúre hemu A bolo presné geometrické usporiadanie na prvom uhlíku na pozícii 3 v kruhu I, teda uhlíku viazanom na hydroxylovú skupinu. V roku 2005 bolo ukázané, že konfigurácia tohto chirálneho uhlíku je S.[4]
Podobne ako hem B, aj hem A je často naviazaný na apoproteín pomocou koordinačnej väzby medzi atómom železa a bočnými reťazcami zachovaných aminokyselín. V enzýme respiračného reťazca, cytochróm c oxidáze (CCO), je piatym ligandom hemu A, ktorý tvorí reakčné miesto pre kyslík, histidylová skupina.[5] Tento ligand (histidín) sa takisto bežne nachádza aj v iných hemoproteínoch, ako sú hemoglobín a myoglobín.

Ako kofaktor
Príkladom metaloproteínu, ktorý viaže hem A, je cytochróm c oxidáza (CCO). Táto zložitá bielkovina obsahuje hem A na dvoch rôznych miestach, každý s inou finkciou. Jednotlivé miesta sú označované ako cytochróm a a cytochróm a3. Atóm železa v heme A v cytochróme a je hexakoordinovaný, teda viazaný na 6 ďalších atómov. V molekule cytochrómu a3 ja niekedy viazaný na 5 iných atómov (pentakoordinácia), čo necháva voľné šieste väzbové miesto, kam sa môže viazať molekula kyslíku (O2).[6] Okrem toho tento enzým viaže tri ióny mede, horčík, zinok a niekoľko iónov sodíka a draslíka. Predpokladá sa, že tieto dve hemové skupiny si vymieňajú elektróny medzi sebou, iónmi mede a proteínom cytochrómom c poblíž.
Predpokladá sa, že formylová skupina a izoprenoidový bočný reťazec majú v CCO dôležitú úlohu v zachovávaní energie pri redukcii kyslíka. CCO je podľa všetkého zodpovedaná za zachovávanie energie redukcie dikyslíku tým, že pumpuje protóny do intermembránového priestoru mitochondrie. Tento predpoklad bol publikovaný skupinou S. Yoshikawovej.[7]
Referencie
- ↑ Heme A of Cytochrome c Oxidase. Journal of Biological Chemistry, 1975, s. 7602–7622. DOI: 10.1016/S0021-9258(19)40860-0. PMID 170266.
- ↑ Isolation, crystallisation, and synthesis of the dimethyl ester of porphyrin a, the iron-free prosthetic group of cytochrome c oxidase. Journal of the Chemical Society, Perkin Transactions 1, 1985, s. 135. DOI: 10.1039/P19850000135.
- ↑ Cytohämin aus Herzmuskel. Zeitschrift für Physiologische Chemie, 1951, s. 1–4. DOI: 10.1515/bchm2.1951.288.1.1. PMID 14860765.
- ↑ Yamashita E, Aoyama H, Yao M, Muramoto K, Shinzawa-Itoh K, Yoshikawa S, Tsukihara T.; AOYAMA; YAO. Absolute configuration of the hydroxyfarnesylethyl group of heme A, determined by X-ray structural analysis of bovine heart cytochrome c oxidase using methods applicable at 2.8 Angstrom resolution. Acta Crystallographica D, 2005, s. 1373–1377. DOI: 10.1107/S0907444905023358. PMID 16204889.
- ↑ Tsukihara T, Shimokata K, Katayama Y, Shimada H, Muramoto K, Aoyama H, Mochizuki M, Shinzawa-Itoh K, Yamashita E, Yao M, Ishimura Y, Yoshikawa S.; SHIMOKATA; KATAYAMA. The low-spin heme of cytochrome c oxidase as the driving element of the proton-pumping process. PNAS, 2003, s. 15304–15309. DOI: 10.1073/pnas.2635097100. PMID 14673090.
- ↑ a b Redox-Coupled Crystal Structural Changes in Bovine Heart Cytochrome c Oxidase. Science, 1998, s. 1723–1729. Dostupné online. DOI: 10.1126/science.280.5370.1723. PMID 9624044.
- ↑ Shimokata K, Katayama Y, Murayama H, Suematsu M, Tsukihara T, Muramoto K, Aoyama H, Yoshikawa S, Shimada H.; KATAYAMA; MURAYAMA. The proton pumping pathway of bovine heart cytochrome c oxidase. PNAS, 2007, s. 4200–4205. DOI: 10.1073/pnas.0611627104. PMID 17360500.
Pozri aj
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Heme A na anglickej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk
