
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
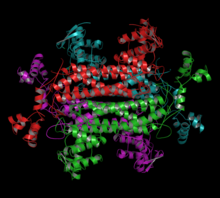 Tetramér fumarázy. | |
| Identifikátory | |
|---|---|
| Číslo EC | EC 4.2.1.2 |
| Číslo CAS | 9032-88-6 |
| Databázy | |
| IntEnz | hľadať v IntEnz |
| BRENDA | hľadať v BRENDA |
| ExPASy | hľadať v ExPASy |
| KEGG | hľadať v KEGG |
| MetaCyc | hľadať v MetaCyc |
| PDB štruktúry | RSCB PDB PDBe PDBsum |
Fumaráza alebo fumaráthydratáza je enzým, ktorý katalyzuje reverzibilnú hydratáciu fumarátu na malát. Fumaráza existuje v dvoch formách: mitochondriálna a cytozolová. Mitochondriálna fumaráza sa účastní Krebsovho cyklu, zatiaľ čo cytozolová fumaráza sa účastní metabolizmu aminokyselín a fumarátu. Subcelulárna lokalizácia enzýmov je daná prítomnosťou signálnej sekvencie na N-konci mitochondriálnej formy, ktorá u cytozolovej formy chýba.[1]
Tento enzým sa účastní dvoch metabolických dráh: citrátového cyklu a reverzného citrátového cyklu (fixácia CO2). Takisto je významný u rakoviny obličiek. Mutácie v tomto géne boli asociované s vývojom leiomyómov v koži a maternici v súvislosti s rakovinou obličiek.[chýba zdroj
Štruktúra
Gén
Fumarázu kóduje gén FH, ktorý sa u ľudí nachádza na chromozomálnej pozícii 1q42.3-q43. Tento gén obsahuje 10 exónov.[1]
Proteín
V kryštálovej štruktúre fumarázy C z Escherichia coli boli objavené dve väzbové miesta pre dikarboxylové kyseliny, ktoré sa nachádzajú blízko seba. Tieto väzbové miesta sa nazývajú aktívne miesto a B miesto a sú prepojené sériou vodíkových mostíkov. Prístup na ktorékoľvek z týchto miest je možný len cez otvor na povrchu enzýmu poblíž B miesta.[2] Aktívne miesto sa skladá z troch domén. Väzbové vrecko vytvorené okolitými reziduami je dostatočné na naviazane molekuly vody i v prípade, že žiadny ligand nie je naviazaný na aktívne miesto.[2] Kryštalografický výskum na B mieste ukázal pohyb His129 medzi voľným a obsadeným stavom. Toto takisto naznačuje, že premena imidazol-imidazólium ovláda prístup na alosterické B miesto.[2]
Subtypy
Existujú dve triedy fumaráz, trieda I a trieda II.[3] Klasifikácia záleží na usporiadaní podjednotiek, prítomnosti kovového iónu a teplotnej stabilite. Fumarázy triedy I menia stav alebo sa stávajú neaktívnymi pri vystavení žiareniu alebo teplote, sú citlivé na superoxidový anión, obsahujú železnatý katión Fe2+ a sú to dimerické proteíny, ktorých podjedotky majú hmotnosť asi 120 kD. Fumarázy triedy II, ktoré sa nachádzajú v prokaryotoch i eukaryotoch, sú tetramérne enzýmy, ktorých podjednotky majú hmotnosť asi 200 kD. Skladajú sa z troch rozličných segmentov s výrazne konzervovanými aminokyselinami, neobsahujú železnatý katión a sú termálne stabilné. Prokaryoty obsahujú tri rôzne formy fumarázy: fumarázu A, fumarázu B a fumarázu C. Fumaráza A a fumaráza B z Escherichia coli sú fumarázy triedy I, zatiaľ čo fumaráza C je fumaráza triedy II.[4]
Funkcia
Mechanizmus
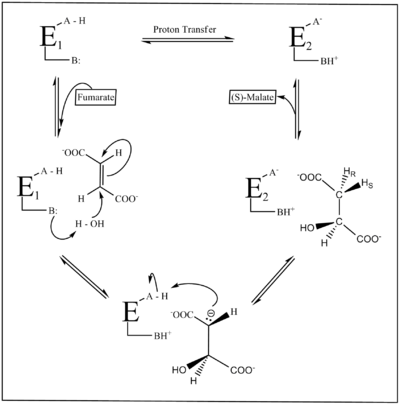
Obrázok 1 ukazuje reakčný mechanizmus fumarázy. Dve reziduá (Asn a Lys) katalyzujú prenos protónu. Ionizačný stav týchto reziduí udáva dve podoby tohto enzýmu: E1 a E2. U E1 existujú v neutrálnej podobe AH/B:, zatiaľ čo v E2 existujú v zwitteriónovej podobe A-/BH+. E1 viaže fumarát a katalyzuje jeho premenu na malát a E2 viaže malát a katalyzuje jeho premenu na fumarát. Pri každom katalytickom cykle musia tieto formy izomerizovať z jednej na druhú.[5]
Napriek biologickej dôležitosti tejto reakcie nie je mechanizmus úplne pochopený. Reakcia sa dá sledovať v oboch smeroch, ale presný postup tvorby fumarátu z malátu nie je presne známy kvôli vysokej hodnote pKa vodíka HR (obrázok 2), ktorý sa odstraňuje bez pomoci kofaktorov či koenzýmov. Reakcia z fumarátu na malát je jasnejšia a zahŕňa stereošpecifickú hydratáciu fumarátu za vzniku S-malátu pomocou trans-adície hydroxylovej skupiny a vodíkového atómu. Prvé výskumy tejto reakcie naznačovali, že tvorba fumarátu z malátu sa skladá z dehydratácie malátu a vzniku karbokatiónu, ktorý následne stráca alfa-protón za vzniku fumarátu. Na základe toho sa predpokladalo, že tvorba malátu z fumarátu prebieha opačne ako E1 eliminácia - cez protonáciu fumarátu, čím by vznikol karbokatión, a následnou adíciou hydroxylovej skupiny z vody. Novšie štúdie však ukázali, že mechanizmus v skutočnosti prebieha cez acidobázicky katalyzovanú elimináciu a karbanión, teda ako E1cB eliminácia (obrázok 1).[5][6][7]

Biochemické dráhy
V citrátovom cykle je funkciou fumarázy sprostredkovať medzikrok pre tvorbu energie v podobe NADH.[8] V cytozole tento enzým metabolizuje fumarát, ktorý vzniká ako vedľajší produkt močovinového cyklu a katabolizmu aminokyselín. Štúdie ukázali, že aktívne miesto enzýmu sa skladá z reziduí aminokyselín pochádzajúcich z troch zo štyroch podjednotiek tetramérneho enzýmu.[4][5][6][7]
Iné substráty
Hlavnými substrátmi fumarázy sú fumarát a malát. Okrem toho je však tento enzým schopný katalyzovať i dehydratáciu D-vínanu, pri ktorej vzniká enol-oxalacetát. Enol-oxalacetát potom izomerizuje na keto-oxalacetát. Fumaráza A i fumaráza B majú prakticky rovnakú kinetiku reverzibilnej premeny malátu na fumarát, ale fumaráza B má omnoho vyššiu katalytickú účinnosť premeny D-vínanu na oxalacetát oproti fumaráze A.[9] Vďaka tomu môžu baktérie ako E. coli využiť D-vínan na rast. Rast mutantov, ktorí nemali funkčný gén fumB kódujúci fumarázu B bol však výrazne pomalší.[9]
Klinický význam
Nedostatok fumarázy je charakterizovaný polyhydramniom (nadbytkom plodovej vody) a abnormalitami mozgu plodu. U novorodencov sa vyskytujú vážne neurologické abnormality, slabé kŕmenie a slabé svaly. Zvýšená kyselina fumarová v moči naznačuje nedostatok fumarázy. Aktuálne už je možné nedostatok fumarázy testovať i geneticky.[3]
Fumaráza je hojne prítomná v tkanive plodu i dospelého. Veľké percento enzýmu sa exprimuje v koži, prištítnom teliesku, lymfe a hrubom čreve.
Referencie
- ↑ a b FH (fumarate hydratase)
- ↑ a b c Weaver T. Structure of free fumarase C from Escherichia coli. Acta Crystallogr. D, October 2005, s. 1395–401. DOI: 10.1107/S0907444905024194. PMID 16204892.
- ↑ a b FH (fumarate hydratase). . Atlas of Genetics and Cytogenetics in Oncology and Haematology, 2006-07-01. Dostupné online.
- ↑ a b X-ray crystallographic and kinetic correlation of a clinically observed human fumarase mutation. Protein Sci., June 2002, s. 1552–7. DOI: 10.1110/ps.0201502. PMID 12021453.
- ↑ a b c HEGEMONY, Adrian D.; FREY, Perry A.. Enzymatic reaction mechanisms. Oxford : Oxford University Press, 2007. ISBN 978-0-19-512258-9.
- ↑ a b BEGLEY, Tadhg P.; MCMURRY, John. The organic chemistry of biological pathways. : Roberts and Co. Publishers, 2005. ISBN 978-0-9747077-1-6.
- ↑ a b Enzymatic reaction mechanisms. San Francisco : W. H. Freeman, 1979. ISBN 978-0-7167-0070-8.
- ↑ Fumarase: a paradigm of dual targeting and dual localized functions. The FEBS Journal, 2011, s. 4230–42. DOI: 10.1111/j.1742-4658.2011.08359.x. PMID 21929734.
- ↑ a b Biochemical similarities and differences between the catalytic cluster containing fumarases FumA and FumB from Escherichia coli. PLOS ONE, February 26, 2021, s. e55549. DOI: 10.1371/journal.pone.0055549. PMID 23405168.
Iné projekty
 Commons ponúka multimediálne súbory na tému Fumaráza
Commons ponúka multimediálne súbory na tému Fumaráza
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Fumarase na anglickej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk
