
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Izoleucín | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C6H13NO2 |
| Systematický názov | Kyselina (2S,3S)-2-amino-3-metylpentánová |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 131,175 g/mol |
| Ďalšie informácie | |
| Číslo CAS | L: 73-32-5 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Izoleucín (skratka Ile alebo I[1]) je α-aminokyselina, ktorá sa objavuje pri biosyntéze bielkovín. Obsahuje α-aminoskupinu (ktorá je za fyziologických podmienok v protónovanom stave −NH3+), α-karboxylovú skupinu (ktorá je za fyziologických podmienok v deprotónovanej forme −COO-) a uhľovodíkový bočný reťazec (s centrálnym atómom uhlíka viazanom na tri ďalšie atómy uhlíka). Je klasifikovaný ako nepolárna, nenabitá (pri fyziologickom pH), alifatická aminokyselina s rozvetveným reťazcom. Pre ľudí je nevyhnutný, čo znamená, že telo si ho nedokáže syntetizovať a musí byť prijímané v strave. Izoleucín sa syntetizuje z pyruvátu pomocou enzýmov biosyntézy leucínu v iných organizmoch, ako sú baktérie.[2] Je kódovaný kodónmi AUU, AUC a AUA.
Izoleucín je konštitučný izomér leucínu. Sú to jediné dve proteinogénne aminokyseliny s rovnakým sumárnym vzorcom, čo komplikuje ich rozlíšenie pri stanovení hmotnostnou spektrometriou peptidov.
Chemická syntéza
Izoleucín je možné syntetizovať viacstupňovým postupom z 2-brómbutánu a dietylmalonátu.[3] Syntetický izoleucín bol pôvodne opísaný v roku 1905 francúzskym chemikom Louisom Bouveaultom.[4]
Nemecký chemik Felix Ehrlich objavil izoleucín v roku 1903 v hemoglobíne.[chýba zdroj
Metabolizmus
Biosyntéza
Izoleucín je esenciálna aminokyselina, takže sa v tele nesyntetizuje, preto sa musí prijímať v strave, zvyčajne ako súčasť bielkovín. V rastlinách a mikroorganizmoch sa syntetizuje v niekoľkých krokoch, počínajúc pyruvátom a alfa-ketobutyrátom. Enzýmy zapojené do tejto biosyntézy sú:[5]
- Acetolaktátsyntáza
- Izomeroreduktáza acetohydroxykyselín
- Dehydratáza dihydroxykyselín
- Valínaminotransferáza
Katabolizmus
Izoleucín je glukogénna aj ketogénna aminokyselina. Po transaminácii s alfa-ketoglutarátom sa uhlíkový skelet oxiduje a štiepi na propionyl-CoA a acetyl-CoA. Propionyl-CoA sa premieňa na sukcinyl-CoA, jeden z medziproduktov citrátového cyklu, ktorý sa môže premeniť na oxaloacetát a vstúpiť do glukoneogenézy (preto je izoleucín glukogénny). U cicavcov sa acetyl-CoA nemôže premeniť na uhľohydráty, ale môže vstúpiť do citrátového kondenzáciou s oxaloacetátom za vzniku citrátu, takisto sa môže použiť pri syntéze ketolátok (preto je izoleucín aj ketogénny) alebo mastných kyselín.[6]
Rezistencia na inzulín
Izoleucín, podobne ako iné aminokyseliny s rozvetveným reťazcom, je spojený s inzulínovou rezistenciou: v krvi diabetických myší, potkanov a ľudí sú pozorované vyššie hladiny izoleucínu.[7] Myši kŕmené jeden deň izoleucínovou deprivačnou diétou mali zlepšenú citlivosť na inzulín a kŕmenie izoleucínovou deprivačnou diétou počas jedného týždňa výrazne znížilo hladinu glukózy v krvi.[8] U obéznych myší (ktorých obezita bola dosiahnutá pomocou stravy) a myší rezistentných na inzulín mala diéta so zníženými hladinami izoleucínu (s alebo bez iných aminokyselín s rozvetveným reťazcom) za následok zníženie adipozity a zlepšenie citlivosti na inzulín.[9][10] Pre priaznivé metabolické účinky nízkobielkovinovej diéty sú potrebné nižšie hladiny izoleucínu v strave.[10] U ľudí diéta s obmedzeným množstvom bielkovín znižuje hladinu izoleucínu v krvi a znižuje hladinu glukózy v krvi nalačno.[11] Vyššia hladina izoleucínu v strave je u ľudí spojená s vyšším indexom telesnej hmotnosti.[10]
Zdroje v potrave a význam
Aj keď sa táto aminokyselina u zvierat nevytvára, uchováva sa vo veľkých množstvách. Potraviny s vysokým obsahom izoleucínu zahŕňajú vajcia, sójový proteín, morské riasy, morčacie mäso, kuracie mäso, jahňacie mäso, syry a ryby.[12]
Výbor pre potravu a výživu (FNB) amerického Inštitútu medicíny stanovil odporúčané denné dávky pre esenciálne aminokyseliny v roku 2002. V prípade izoleucínu je to pre dospelých vo veku 19 rokov a starších 19 mg/kg telesnej hmotnosti/deň.[13]
Okrem svojej biologickej úlohy ako živiny sa ukázalo, že izoleucín sa podieľa aj na regulácii metabolizmu glukózy.[14]
Niektoré zdroje uvádzajú, že izoleucín znižuje únavu,[15] avšak podľa review z roku 2019 nemajú BCAA výrazný efekt na zníženie únavy.[16] Pomáhajú však so znížením hladiny laktátu (ktorý vzniká počas cvičenia a jeho hromadenie v svaloch sa prejavuje ako svalovica) a okrem toho pomáhajú regulovať hladiny amoniaku (ktorý spolu s laktátom spôsobuje únavu), glukózy, voľných mastných kyselín a kreatínkinázy.[16]
Izoméry
Izoleucín je jednou z dvoch proteinogénnych aminokyselín, ktoré majú dve chirálne centrá. Druhou je treonín. Prítomnosť dvoch chirálnych centier v tomto prípade vedie k celkom štyrom rôznym izomérom podľa Le Belovho-van ’t Hoffov vzťahu. V živých systémoch je prítomný len L-izoleucín.
Izoleucín je konštitučný izomér leucínu.
Z izoméru L-aloizoleucínu sa syntetizuje kyselina koronamová, ktorá je súčasťou fytotoxínu koronatínu, ktorý produkuje baktéria Pseudomonas syringae.[17] Ako aloizoleucín vzniká nie je známe.
| Izoméry izoleucínu | |||||||
|---|---|---|---|---|---|---|---|
| Triviálny názov | izoleucín | d-izoleucín | l-izoleucín | dl-izoleucín | d-aloizoleucín | l-aloizoleucín | dl-aloizoleucín |
| Synonymum | (R)-izoleucín | L-(+)-izoleucín | (R*,R*)-izoleucín | aloizoleucín | |||
| CAS číslo | 443-79-8 | 319-78-8 | 73-32-5 | 1509-35-9 | 1509-34-8 | 3107-04-8 | |
 
|
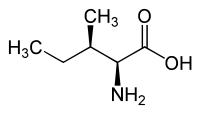
| L-izoleucín (2S,3S) a D-izoleucín (2R,3R) |
|
| L-aloizoleucín (2S,3R) a D-aloizoleucín (2R,3S) |
Referencie
- ↑ Nomenclature and Symbolism for Amino Acids and Peptides . IUPAC-IUB Joint Commission on Biochemical Nomenclature, 1983. Dostupné online. Archivované 2008-10-09 z originálu.
- ↑ Pathway for isoleucine formation form pyruvate by leucine biosynthetic enzymes in leucine-accumulating isoleucine revertants of Serratia marcescens. Journal of Biochemistry, July 1977, s. 95–103. DOI: 10.1093/oxfordjournals.jbchem.a131698. PMID 142769.
- ↑ dl-ISOLEUCINE. Organic Syntheses, 1941, roč. 21, s. 60. Dostupné online . ISSN 0078-6209. DOI: 10.15227/orgsyn.021.0060. (po anglicky)
- ↑ Action du sodium sur les éthers des acides monobasiques à fonction simple de la série grasse. Compt. Rend., 1905, s. 1593–1595. Dostupné online. (po francúzsky)
- ↑ LEHNINGER, Albert L.. Lehninger principles of biochemistry.. New York : Worth Publishers, 2000. (3rd ed..) Dostupné online. ISBN 1-57259-153-6.
- ↑ COLE, Jeffrey T.. Branched Chain Amino Acids in Clinical Nutrition. : , 14 November 2014. ISBN 978-1-4939-1923-9. Chapter 2: Metabolism of BCAAs.
- ↑ Branched-chain amino acids in metabolic signalling and insulin resistance. Nature Reviews. Endocrinology, December 2014, s. 723–36. DOI: 10.1038/nrendo.2014.171. PMID 25287287.
- ↑ Effects of individual branched-chain amino acids deprivation on insulin sensitivity and glucose metabolism in mice. Metabolism, June 2014, s. 841–50. DOI: 10.1016/j.metabol.2014.03.006. PMID 24684822.
- ↑ Restoration of metabolic health by decreased consumption of branched-chain amino acids. The Journal of Physiology, February 2018, s. 623–645. DOI: 10.1113/JP275075. PMID 29266268.
- ↑ a b c The adverse metabolic effects of branched-chain amino acids are mediated by isoleucine and valine. Cell Metabolism, May 2021, s. 905–922.e6. DOI: 10.1016/j.cmet.2021.03.025. PMID 33887198.
- ↑ Decreased Consumption of Branched-Chain Amino Acids Improves Metabolic Health. Cell Reports, July 2016, s. 520–530. DOI: 10.1016/j.celrep.2016.05.092. PMID 27346343.
- ↑ Foods highest in Isoleucine . Condé Nast. Dostupné online.
- ↑ INSTITUTE OF MEDICINE. Dietary Reference Intakes for Energy, Carbohydrates, Fiber, Fat, Fatty Acids, Cholesterol, Protein, and Amino Acids. Washington, DC : The National Academies Press, 2002. Dostupné online. ISBN 978-0-309-08525-0. DOI:10.17226/10490 Protein and Amino Acids, s. 589–768.
- ↑ YOSHIZAWA, Fumiaki. Effects of Leucine and Isoleucine on Glucose Metabolism. : , October 2015. Dostupné online. ISBN 978-1-4939-1922-2. DOI:10.1007/978-1-4939-1923-9_6 S. 63–73.
- ↑ BCAA - Ako vybrať najlepšie aminokyseliny ? Dávkovanie a Ceny . Fitgo, . Dostupné online.
- ↑ a b HORMOZNEJAD, Razie; ZARE JAVID, Ahmad; MANSOORI, Anahita. Effect of BCAA supplementation on central fatigue, energy metabolism substrate and muscle damage to the exercise: a systematic review with meta-analysis. Sport Sciences for Health, 2019-08-01, roč. 15, čís. 2, s. 265–279. Dostupné online . ISSN 1825-1234. DOI: 10.1007/s11332-019-00542-4. (po anglicky)
- ↑ VAILLANCOURT, Frédéric H.; YEH, Ellen; VOSBURG, David A.. Cryptic chlorination by a non-haem iron enzyme during cyclopropyl amino acid biosynthesis. Nature, 2005-08, s. 1191–1194. Dostupné online. ISSN 1476-4687. DOI: 10.1038/nature03797. (po anglicky)
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Isoleucine na anglickej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk


