
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Jodid fosforitý | |||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||||
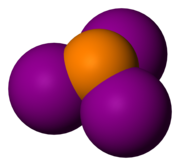
| Sumárny vzorec | PI3 | ||||||||||||||||||||||||||||||||||
| Vzhľad | temne červená kryštalická látka | ||||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 411,7 u | ||||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 411,68717 g/mol | ||||||||||||||||||||||||||||||||||
| Teplota topenia | 61,2 °C | ||||||||||||||||||||||||||||||||||
| Teplota rozkladu | 200 °C | ||||||||||||||||||||||||||||||||||
| Hustota | 4,18 g/cm3 | ||||||||||||||||||||||||||||||||||
| Rozpustnosť | Rozkladá sa vo vode | ||||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | -46 kJ/mol | ||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||||
| Číslo CAS | 13455-01-1 | ||||||||||||||||||||||||||||||||||
| Číslo UN | 3260 | ||||||||||||||||||||||||||||||||||
| EINECS číslo | 236-647-2 | ||||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||||
Jodid fosforitý (PI3) je anorganická zlúčenina fosforu a jódu. Za bežných podmienok sa jedná o nestabilnú temne červenú kryštalickú látku, ktorá prudko reaguje s vodou. Je pomerne rozšíreným omylom,[1] že je jodid fosforitý príliš nestabilný na to, aby sa dal skladovať. V skutočnosti je bežne v predaji. Široko sa používa v organickej chémii pre konverziu alkoholov na alkyljodidy. Je tiež silným redukčným činidlom. Fosfor tvorí s jódom tiež tetrajóddifosfán (P2I4), existencia jodidu fosforečného (PI5) pri izbovej teplote je však nejasná, skôr sa jedná o kokrystalizát jodidu fosforitého s jódom.[2]
Vlastnosti
Jodid fosforitý má rozpustený v sírouhlíka v zásade nulový dipólový moment, pretože väzba PI nemá takmer vôbec dipólový charakter. Táto väzba je navyše slabá, PI3 je oveľa menej stabilná ako iné fosforečné halogenidy; Štandardné zlučovacie entalpia je len -46kJ/mol (pevná látka). Atóm fosforu má v nukleárnej magnetickej rezonančnej spektroskopii posun 178 pm (vyššia frekvencia než kyseliny trihydrogenfosforečnej).
Reakcia
Jodid fosforitý búrlivo reaguje s vodou za vzniku kyseliny fosforitej (H3PO3) a jodovodíkovej (HI), uvoľňujú sa tiež malé množstvá fosfánu a zlúčenín P-P. S alkoholy tvorí alkyljodidy; táto reakcia je hlavnou oblasťou použitia jodidu fosforitého.
Jodid fosforitý má tiež silné redukčné účinkami. Redukuje sulfoxidy na tioétery, a to aj pri -78° C.[3] Zahrievanie roztoku jodidu fosforité v 1-jódbután s červeným fosforom vyvoláva redukciu na tetrajóddifosfán( P2I4).
Príprava
Obvyklou metódou prípravy jodidu fosforitého je priama reakcia prvkov, väčšinou pridávaním jódu do roztoku bieleho fosforu v sirouhlíku:
- P4 + 6 I2 → 4 PI3
Možno tiež využiť prevod chloridu fosforitého (PCl3) na jodid fosforitý pôsobením jodovodíka alebo niektorých kovových jodidov.
Použitie
Jodid fosforitý sa používa v laboratóriu pre konverziu primárnych alebo sekundárnych alkoholov na alkyljodidy.[4] Alkohol je tu mnohokrát nielen reaktantom ale aj rozpúšťadlom. Jodid fosforitý sa často generuje in situ reakciou červeného fosforu s jódom za prítomnosti alkoholu. Napríklad konverzií metylalkoholu možno získať jódmetán:
- PI3 + 3 CH3OH → 3 CH3I + H3PO3
Alkyljodidy sú zlúčeniny užitočné pre nukleofilné substitučné reakcie a pre prípravu Grignardových reagencií.
Podobné látky
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Jodid fosforitý na českej Wikipédii.
Referencie
- ↑ WADE, L. G., Jr.. Organic Chemistry. 6. ilustrované vyd. Upper Saddle River (New Jersey, USA) : Pearson/Prentice Hall, 2005. ISBN 978-0-131-47871-8. S. 477. (po anglicky)
- ↑ HOLLEMAN, Arnold Frederik; WIBERG, Nils. Lehrbuch der Anorganischen Chemie. 102. vyd. Berlín (Nemecko) : Auflage, de Gruyter, 2007. ISBN 978-3-11-017770-1. (po nemecky)
- ↑ DENIS, Jean Noel; KRIEF, Alain. Phosphorus tri-iodide (PI3), a powerful deoxygenating agent. Journal of the Chemical Society, Chemical Communications, december 1980, s. 544–5. DOI: 10.1039/C39800000544. (po anglicky)
- ↑ FURNELL, B. S., et al. Vogel's Textbook of Practical Organic Chemistry. 5. vyd. New York (USA) : Longman/Wiley, 1989. ISBN 0-582-46236-3. (po anglicky)
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk




