
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Chlorid seleničitý | |
|---|---|
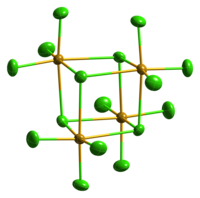 Tetramerní jednotka chloridu seleničitého | |
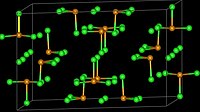 Krystalová struktura chloridu seleničitého | |
| Obecné | |
| Systematický název | Chlorid seleničitý |
| Anglický název | Selenium tetrachloride |
| Německý název | Selentetrachlorid |
| Sumární vzorec | SeCl4 |
| Vzhled | bílé až žluté krystaly |
| Identifikace | |
| Registrační číslo CAS | 10026-03-6 |
| PubChem | 66205 |
| SMILES | Cl(Cl)(Cl)Cl |
| InChI | 1S/Cl4Se/c1-5(2,3)4 |
| Vlastnosti | |
| Molární hmotnost | 220,771 g/mol |
| Teplota tání | 191,4 °C (sublimuje) |
| Hustota | 2,6 g.cm−3 |
| Rozpustnost ve vodě | rozkládá se |
Některá data mohou pocházet z datové položky. | |
Chlorid seleničitý, SeCl4, je anorganická sloučenina selenu a chloru. Tvoří žluté až bílé těkavé krystaly. Je jedním ze dvou běžných chloridů selenu, druhým je Se2Cl2. Využívá se při syntéze sloučenin selenu.
Příprava
Připravuje se přímou reakcí selenu s chlorem.[1] Při zahřívání dochází k sublimaci produktu. Těkavosti chloridu je možné využít k čištění selenu.
Struktura
Pevný SeCl4 vytváří tetramerní kubickou strukturu.[1] Atomy selenu tvořící oktaedry SeCl6 obsazují čtyři vrcholy krychle, zbylé čtyři jsou tvořeny můstkovými chloridy. Můstkové vazby Se-Cl jsou delší než terminální vazby Se-Cl, úhly Cl-Se-Cl jsou přibližně 90°.[2]
Reakce
V přítomnosti vody hydrolyzuje za vzniku kyseliny seleničité:[3]
- SeCl4 + 3 H2O → H2SeO3 + 4 HCl
S chloridy alkalických kovů v prostředí koncentrované HCl poskytuje komplexní sloučeniny:[4]
- SeCl4 + 2 KCl → K2
S chloridem hlinitým reaguje za vzniku kationtu SeCl +
3 :[4]
- SeCl4 + AlCl3 → SeCl +
3 + AlCl −
4
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Selenium tetrachloride na anglické Wikipedii.
- ↑ a b GREENWOOD, Norman Neill. Chemie prvků. Sv. 1.. 1. vyd. vyd. Praha: Informatorium 793 s., 1 příl s. ISBN 80-85427-38-9, ISBN 978-80-85427-38-7. S. 947–948.
- ↑ KNIEP, Rüdiger; KÖRTE, Lutz; MOOTZ, Dietrich. Kristallstruktur der stabilen Modifikation von SeCl 4 / Crystal Structure of the Stable Modification of SeCl 4. Zeitschrift für Naturforschung B. 1981-12-01, roč. 36, čís. 12, s. 1660–1662. Dostupné online . ISSN 1865-7117. DOI 10.1515/znb-1981-1231. (anglicky)
- ↑ Chemical Papers. www.chemicalpapers.com . . Dostupné online.
- ↑ a b HOUSECROFT, Catherine E. Anorganická chemie. Vyd. 1. vyd. Praha: Vysoká škola chemicko-technologická v Praze xxx, 1119 s. s. ISBN 978-80-7080-872-6, ISBN 80-7080-872-1. S. 558.
Externí odkazy
 Obrázky, zvuky či videa k tématu Chlorid seleničitý na Wikimedia Commons
Obrázky, zvuky či videa k tématu Chlorid seleničitý na Wikimedia Commons
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk
