
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
Sukcinát dehydrogenáza (SDH), též mitochondriální komplex II (CII) nebo sukcinát-ubichinon oxidoreduktáza (SQR) je enzymatický komplex přítomný v mitochondriích eukaryot a v bakteriálních buňkách. Tento komplex katalyzuje oxidaci sukcinátu na fumarát za současné redukce ubichinonu na ubichinol.[1] Sukcinát dehydrogenáza je tedy řazena mezi oxidoreduktázy. SDH ale zároveň dodává elektrony ze sukcinátu do elektron transportního řetězce. Díky tomu tvoří pomyslnou křižovatku mezi dvěma pro buňku nezbytnými energetickými procesy - citrátovým (Krebsovým) cyklem a dýchacím řetězcem. SDH je také jediným enzymem citrátového cyklu, který není volně v mitochondriální matrix, ale je ukotven ve vnitřní membráně mitochondrií.[2]
Struktura
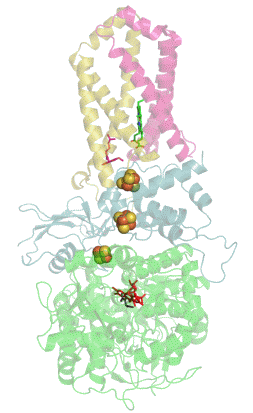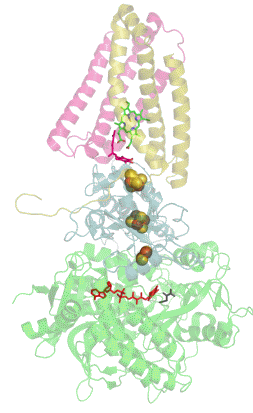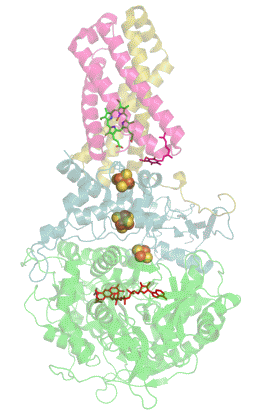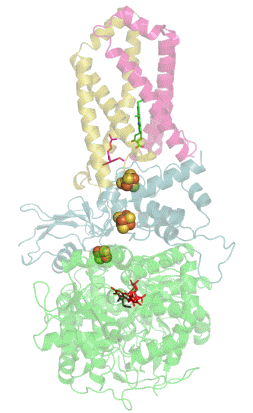
Sukcinát dehydrogenáza se skládá ze čtyř různých podjednotek označených jako SDHA, SDHB, SDHC a SDHD (Obrázek 1). Sestavený komplex obsahuje dvě morfologicky odlišné části - hydrofilní část tvořenou SDHA a SDHB, kde dochází k enzymatické aktivitě, a hydrofobní část z podjednotek SDHC a SDHD, která ukotvuje celý komplex ve vnitřní mitochondriální membráně.[3]
SDHA je flavoproteinem, obsahuje tedy kovalentně navázaný kofaktor flavin adenin dinukleotid (FAD), což je derivát vitamínu B2 (riboflavinu). Důležitým kofaktorem podjednotky SDHB jsou tři Fe-S klastry , a . SDHB spojuje katalytickou podjednotku SDHA s hydrofobní kotvou, která je tvořena z pojednotek SDHC a SDHD, mezi něž je vložena molekula hemu b, která zřejmě slouží ke stabilizaci (Obrázek 1).[4]
Kromě vazebného místo pro sukcinát (na podjednotce SDHA) obsahuje sukcinát dehydrogenáza hlavní vazebné místo pro ubichinon na pomezí podjednotek SDHB, SDHC a SDHD (Obrázek 1).
Skládání a maturace
Všechny podjednotky sukcinát dehydrogenázy jsou kódovány v jaderném genomu, musí být tedy po translaci translokovány do mitochondriální matrix, kde dochází k poskládání celého komplexu. Na podjednotku SDHA je po přesunu do mitochondrie kovalentně navázán kofaktor FAD, k čemuž je zapotřebí dalšího proteinu - asemblačního faktoru sukcinát dehydrogenázy 2 - SDHAF2. Další asemblační faktor - SDHAF4 - chrání monomerní podjednotku SDHA a napomáhá jejímu spojení s SDHB.[4]
Do podjednotky SDHB jsou mitochondriálními proteinovými komplexy vloženy Fe-S klastry, které jsou ovšem náchylné na působení kyslíkových radikálů, dokud není celý komplex SDH poskládán. K její ochraně před radikály slouží další dva asemblační faktory - SDHAF1 a SDHAF3.[4] Žádný z výše zmíněných asemblačních faktorů ovšem není součástí maturované funkční SDH.
Nakonec je dimer SDHA-SDHB spojen s hydrofobními podjednotkami SDHC a SDHD, mezi něž je neznámým způsobem vložena molekula hemu b.
Mechanismus funkce

Enzymatická funkce sukcinát dehydrogenázy spočívá v katalýze oxidace sukcinátu a následném přenosu elektronů na molekulu ubichinonu (Obrázek 3). Molekula sukcinátu je vodíkovými vazbami stabilizována v aktivním místě podjednotky SDHA. Jeden z uhlíků molekuly sukcinátu je poté deprotonován a kofaktor FAD přijme hydrid z dalšího uhlíku molekuly. Tím ze sukcinátu vzniká fumarát a FAD je redukován na FADH2 (Obrázek 4).

Elektrony z molekuly FADH2 jsou poté přesouvány mezi jednotlivými Fe-S klastry podjednotky SDHB až do ubichinon vazebného místa. Poslední klastr poté předává elektrony na ubichinon, který je redukován na ubichinol. Ten dále přenáší elektrony v rámci dýchacího řetězce.
Činnost enzymu je inhibována malonátem, který má totiž podobnou stavbu jako sukcinát a působí tak kompetitivně inhibičně.[2] Také oxalacetát má inhibiční účinky.[5]
Reference
- ↑ Oxford dictionary of biochemistry and molecular biology; revised edition. Příprava vydání R. Cammack et al. New York: Oxford university press, 2006. ISBN 0-19-852917-1.
- ↑ a b VOET, Donald; VOET, Judith. Biochemie. 1.. vyd. Praha: Victoria Publishing, 1995. ISBN 80-85605-44-9.
- ↑ Sun F, Huo X, Zhai Y, Wang A, Xu J, Su D, Bartlam M, Rao Z. Crystal Structure of Mitochondrial Respiratory Membrane Protein Complex II. Cell . 1. 6. 2005 . Dostupné online. DOI 10.1016/j.cell.2005.05.025. PMID 15989954.
- ↑ a b c Van Vranken JG, Na U, Winge DR, Rutter J. Protein-mediated assembly of succinate dehydrogenase and its cofactors. Critical Reviews in Biochemistry and Molecular Biology . 2015 . Dostupné online. DOI 10.3109/10409238.2014.990556. PMID 25488574.
- ↑ Robert K. Murray; Daryl K. Granner; Joe C. Davis; Peter A. Mayes; Victor W. Rodwell. Harper’s Illustrated Biochemistry; twenty-sixth edition. : , 2003. ISBN 0-07-138901-6.
Externí odkazy
 Obrázky, zvuky či videa k tématu Sukcinátdehydrogenáza na Wikimedia Commons
Obrázky, zvuky či videa k tématu Sukcinátdehydrogenáza na Wikimedia Commons
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk
