A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Oxid chloričitý | |||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||
| Sumárny vzorec | ClO2 | ||||||||||||||||||||||||||||||
| Synonymá | E 926 | ||||||||||||||||||||||||||||||
| Vzhľad | žlto-zelený plyn | ||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||
| Molárna hmotnosť | 67,45 g·mol−1 | ||||||||||||||||||||||||||||||
| Teplota topenia | −59 °C | ||||||||||||||||||||||||||||||
| Teplota varu | 11 °C | ||||||||||||||||||||||||||||||
| Hustota | 2,757 g/dm3 | ||||||||||||||||||||||||||||||
| Rozpustnosť | 8 g/dm3 vo vode pri 20 °C rozpustný aj vo vodných roztokoch minerálnych kyselín | ||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | 104,60 kJ/mol | ||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||
| Číslo CAS | 10049-04-4 | ||||||||||||||||||||||||||||||
| Číslo UN | 9191 | ||||||||||||||||||||||||||||||
| EINECS číslo | 233-162-8 | ||||||||||||||||||||||||||||||
| Číslo RTECS | FO3000000 | ||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||
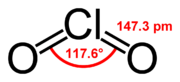
Oxid chloričitý je anorganická chemická zlúčenina. Za normálnych podmienok sa jedná o žlto-zelený ostro štipľavo zapáchajúci plyn. Tuhne pri -59 °C, kedy vytvára jasnooranžové kryštály. Pri vyšších koncentráciách je v plynnom skupenstve nestabilný a rozkladá sa. Využíva sa ako oxidovadlo, na bielenie, pri úprave vody a pri dezifekcii (aj v potravinárstve pod E číslom E 926).
Príprava
Kvôli jeho nestabilite sa väčšinou uprednostňujú spôsoby kde oxid chloričitý vzniká rozpustený v roztoku.
Oxidáciou chloritanov
Oxid chloričitý môžeme v laboratóriu pripraviť chloritanu sodného pomocou chlóru:[1]
2 NaClO2 + Cl2 → 2 ClO2 + 2 NaCl
Okrem toho sa dá pripraviť aj reakciou s chloritanu sodného s kyselinou chlorovodíkovou:
5 NaClO2 + 4 HCl → 5 NaCl + 4 ClO2 + 2 H2O
Pri použití aj tretieho reaktantu - chlórnanu sodného je spotreba kyseliny chlorovodíkovej nižšia:
2 NaClO2 + 2 HCl + NaClO → 2 ClO2 + 3 NaCl + H2O
Redukciou chlorečnanov
V laboratóriu výrobe sa zväčša na výrobu z chlorečnanov používa reakcia medzi chlorečnanom draselným s kyselinou šťaveľovou:
2 KClO3 + 2 H2C2O4 → K2C2O4 + 2 ClO2 + 2 CO2 + H2O
Niekedy aj za prítomnosti kyseliny sírovej:
2 KClO3 + H2C2O4 + 2 H2SO4 → 2 KHSO4 + 2 ClO2 + 2 CO2 + 2 H2O
Priemyselne sa približne 95 % oxidu chloričitého pripravuje pomcou redukcie chlorečnanu sodného. Ako redukovadlo sa v takomto prípade používajú látky ako kyselina chlorovodíková, peroxid vodíka, metanol a oxid siričitý.[2] Moderné spôsoby priemyselnej výroby využívajú najmä metanol a peroxid vodíka, pretože pri použití týchto reaktantov nevzniká nežiadúci vedlajší produkt - chlór a takéto spôsoby výroby sú ekonomicky najvýhodnejšie.
Využitie
Bielenie
Oxid chloričitý sa používa na bielenie buničiny pri výrobe papieru z dreva niekedy aj v kombinácii s chlórom. Používaním oxidu chloričitého sa minimalizuje množstvo použitých organických chlórovaných zlúčenín pri výrobe papieru. Okolo 95 % bielenej kraftovej buničiny sa bieli pomocou oxidu chloričitého.[3]
Dezinfekcia
Používa sa aj na dezinfekciu zdravotných nástrojov.
Okrem medicínskeho prostedia sa používa aj na zaplynenie dozretého ovocia, ako napríklad maliny, jahody a čučoriedky, na ochranu pred plesňami a kvasinkami,[4] v EÚ je však jeho používanie zakázané.[5]
Úprava vody
Oxid chloričitý sa v čističkách vôd používa na úpravu pitnej vody. Používa sa pred úpravou vody chlórom, pretože zničí organické nečistoty vo vode z ktorých by pôsobením chlóru mohli vzniknúť halogénderiváty[6], ktoré sú v pitnej vode považované za karcinogénne. Oxid chloričitý je taktiež efektívnejší než chlór na zneškodnenie baktérií z rodu legionella[7]
Chemická stabilita
Pri parciálnom tlaku plynného oxidu chloričitého vyššom než 10 kPa[2], t.j. koncentrácii vyššej než 10 % vo vzduchu pri normálnych podmienkach hrozí riziko rozkladu na kyslík a chlór, ktorý je sprevádzaný výbuchom. Spúšťačom rozkladu môže byť svetlo, teplo, náhlym zvýšením okolitého tlaku. Preto sa s ním skoro nikdy nepracuje vo forme koncentrovaného plynu, ale vo forme roztoku v koncentráciách 0,5 - 10 g/dm3.
Referencie
- ↑ Chlorine(IV) Oxide Inorganic Syntheses (po anglicky)
- ↑ a b Chlorine Oxides and Chlorine Oxygen Acids Ullmann's Encyclopedia of Industrial Chemistry (po anglicky)
- ↑ Trends in World Bleached Chemical Pulp Production: 1990-2005 Aliance for Environmental Technology (po anglicky, archivované na Wayback Machine)
- ↑ Chlorine Dioxide Pouches Can Make Produce Safer and Reduce Spoilage (po anglicky)
- ↑ E926 - Oxid chloričitý Fér potravina (po česky)
- ↑ Trihalomethane formation during chemical oxidation with chlorine, chlorine dioxide and ozone of ten Italian natural waters (po anglicky)
- ↑ Safety and Efficacy of Chlorine Dioxide for Legionella Control in a Hospital Water System Cambridge University Press (po anglicky)
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk