A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
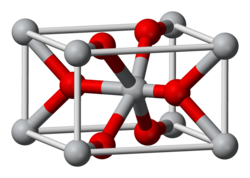
| Oxid manganičitý | |||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||||||
| Sumárny vzorec | MnO2 | ||||||||||||||||||||||||||||||||||||
| Synonymá | Burel | ||||||||||||||||||||||||||||||||||||
| Vzhľad | Hnedočierna práškovitá látka | ||||||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 87,0 u | ||||||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 86,937 g/mol | ||||||||||||||||||||||||||||||||||||
| Teplota rozkladu | 535 °C | ||||||||||||||||||||||||||||||||||||
| Hustota | 5,03 – 5,08 g/cm³ | ||||||||||||||||||||||||||||||||||||
| Rozpustnosť | vo vode: nerozpustný v polárnych rozpúšťadlách: kyselina chlorovodíková kyselina sírová kyselina dusičná (nerozpustný) | ||||||||||||||||||||||||||||||||||||
| Teplota vzplanutia | 535 °C | ||||||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | −520,9 kJ/mol | ||||||||||||||||||||||||||||||||||||
| Štandardná entropia | 53,1 J K−1 mol−1 | ||||||||||||||||||||||||||||||||||||
| Štandardná Gibbsová energia | −466,0 kJ/mol | ||||||||||||||||||||||||||||||||||||
| Merná tepelná kapacita | 0,623 J K−1 g−1 | ||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||||||
| Číslo CAS | 1313-13-9 | ||||||||||||||||||||||||||||||||||||
| Číslo UN | 1479 | ||||||||||||||||||||||||||||||||||||
| EINECS číslo | 215-202-6 | ||||||||||||||||||||||||||||||||||||
| Číslo RTECS | OP0350000 | ||||||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||||||
Oxid manganičitý je jedným z oxidov mangánu. V prírode sa vyskytuje ako černastý alebo hnedý minerál pyroluzit. Čistý oxid manganičitý je čierna práškovitá látka s výraznými redoxnými schopnosťami, nerozpustný vo vode ani v kyseline dusičnej. Je dobre rozpustný v kyseline chlorovodíkovej za studena a za tepla v kyseline sírovej a hydroxide draselnom.
Fyzikálno-chemické vlastnosti
Oxid manganičitý sa pri teplote 535 °C rozkladá za vzniku oxidu manganitého a kyslíka. Pri teplotách blízkych 1000 °C pokračuje rozklad na podvojnú zlúčeninu oxid manganato-manganitého. Pri ešte vyšších teplotách pokračuje rozklad na oxid manganatý.
- 4 MnO2 t → 2 Mn2O3 + O2
- 6 Mn2O3 t → 4 Mn3O4 + O2
- 2 Mn3O4 t → 6 MnO + O2
Oxid manganičitý má silné redukčné aj oxidačné schopnosti. Pôsobením kyseliny chlorovodíkovej dochádza k jeho redukcii za vzniku manganatej soli a chlóru (túto reakciu využil Carl Wilhelm Scheele k prvej izolácii chlóru v roku 1774):
- MnO2 + 4 HCl → MnCl2 + Cl2 + 2 H2O
Pri pôsobení horúcej kyseliny sírovej na oxid manganičitý dochádza k uvoľneniu kyslíka:
- 2 MnO2 + 2 H2SO4 → 2 MnSO4 + O2 + 2 H2O
Zahriatím hydroxidu draselného s oxidom manganičitým a za prebublávania vzduchu dochádza k oxidácii na manganan draselný, ktorý ďalej samovoľne prechádza na manganistan draselný (vďaka oxidu uhličitému vo vzduchu) a vzniknutý oxid manganičitý ďalej reaguje opäť za vzniku mangananu:
- 2 MnO2 + 4 KOH + O2 → 2 K2MnO4 + 2 H2O
- 3 K2MnO4 + 2 CO2 → 2 KMnO4 + 2 K2CO3 + MnO2
Využitie
Redukčné schopnosti sa využívajú pri výrobe manganistanu draselného. Oxidačné schopnosti sa využívali pri výrobe chlóru, horúca kyselina chlorovodíková sa liala na pyroluzit a uvoľňoval sa chlór. Používa sa v alkalických batériách a zinkovo-uhlíkových článkoch v zmesi s uhlíkom ako depolarizačné činidlo, aby sa zabránilo prebíjaniu batérie naprázdno.
Oxid manganičitý sa v laboratóriách využíva na katalyzovaný rozklad peroxidu vodíka na vodu a kyslík:
- 2H2O2 → 2H2O + O2
V organickej syntéze sa využíva k oxidácii allylických alkoholov na príslušné aldehydy alebo ketóny.
- cis-RCH=CHCH2OH + MnO2 → cis-RCH=CHCHO + „MnO“ + H2O
Podobné látky
- Sulfid manganičitý
- Oxid rénatý
- Oxid techničitý
- Oxid manganato-manganitý
- Oxid manganatý
- Oxid manganistý
- Oxid manganitý
Referencie
- ↑ Norman Neil Greenwood, Alan Earnshaw, Chemistry of the Elements, 1nd ed., Butterworth-Heinemann, Oxford : Pergamon, UK, 1997, pp. 1218–20, ISBN 0-08-022057-6.
Pozri aj
Literatúra
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabuľky. 1. vyd. Praha : Grada Publishing, 1999. ISBN 80-7169-855-5.
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Oxid manganičitý na českej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Štruktúrny vzorec
Železo
Abakavir
Aceton
Aminoglykosidy
Amoxicilín
Ampicilín
Analytická chemie
Anglické chemické názvosloví
Anorganická sloučenina
Antibiotikum
Antiseptikum
Atropín
Baktéria
Benzoylperoxid
Bezpilotní letadlo
Brom
Bromičnan draselný
Bromid draselný
Chemická reakce
Chemická sloučenina
Chemický vzorec#Sumárnà vzorec
Chinín
Chlor
Chloramfenikol
Chlorečnan draselný
Chlorid draselný
Chlorid hlinitý
Chloristan draselný
Dihydrogenfosforečnan draselný
Disiřičitan draselný
Dithioničitan draselný
Draslík
Dusík
Dusičnan draselný
Dusitan draselný
Dynamický viskozitní koeficient
Efedrín
Elektrolýza
Ethanol
Ethen
Evropa
Evropská unie
Evropské hospodářské společenství
Fenoxyethanol
Fluor
Fluorid draselný
Fosfor
Fulminát draselný
Fyziologický roztok
Globálně harmonizovaný systém klasifikace a označování chemikálií
Glukóza
Glycerol
H-věty
Halogenidy
Hliník
Hustota
Hydrogenfosforečnan draselný
Hydrogenperoxosíran draselný
Hydrogensíran draselný
Hydrogensiřičitan draselný
Hydroxid draselný
Impetigo
Indexové číslo
International Standard Book Number
Isokyanát draselný
Isothiokyanatan draselný
Ivermektín
Izobarický děj
Jod
Jodičnan draselný
Jodid draselný
Kalciol
Kategorie:Draselné sloučeniny
Kation
Kelvin
Ketamín
Kodeín
Koordinační číslo
Koroze
Krystal
Krystalografická soustava
Krystalografická soustava#KosoÄtvereÄná (ortorombická)
Kyanatan draselný
Kyanid draselný
Kyselina chlorovodíková
Kyselina dusičná
Kyselina L-askorbová
Kyselina listová
Kyselina manganistá
Kyselina octová
Kyselina sírová
Kyselina salicylová
Kyseliny
Kyslík
Laboratoř
Měrná magnetická susceptibilita
Měrná tepelná kapacita
Mangan
Manganan draselný
Manganistan draselný
Manganistan sodný
Metadón
Molární hmotnost
Molární koncentrace
NFPA 704
Nitroglycerín
Omeprazol
Oxidační činidlo
Oxid manganičitý
Oxid manganistý
Oxid olovičitý
Oxid uhličitý
Paracetamol
Peroxid vodíku
Peroxodisíran draselný
Polyethylen
Portál:Chemie
Portál:Obsah
Potassium permanganate?oldid=192811277
Proteosyntéza
Pseudohalogenidy
PubChem
Pyrolýza
Q190865
R-věty
Redoxní reakce
Registrační číslo CAS
Registr toxických účinků chemických látek
Rhenistan draselný
Riboflavín
Ribozóm
Rozpustnost
Roztok
Síra
Síran draselný
Síran draselno-hlinitý
S-věty
Selen
Siřičitan draselný
Slávička mnohotvárná
Směrnice Evropské unie
Soli
Soubor:Manganistan draselný.JPG
Soubor:Potassium-permanganate-solution cropped.png
Soubor:Potassium-permanganate-unit-cell-3D-balls.png
Soustava SI
Speciální:Zdroje knih/80-7169-855-5
Standardní molární entropie
Standardní slučovací entalpie
Standardní slučovací Gibbsova energie
Standardní teplota a tlak
Streptomycín
Stupeň Celsia
Sulfan
Systematický název
Tellur
Teplota vznícení
Thiokyanatan draselný
Tiamín
Titrace
Triviální název
Tuberkulóza
Uhlík
UN kód
Vodík
Voda
Wikimedia Commons
Wikipedie:WikiProjekt Překlad/Rady
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk





