
A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Tomuto článku alebo sekcii chýbajú odkazy na spoľahlivé zdroje, môže preto obsahovať informácie, ktoré je potrebné ešte overiť. Pomôžte Wikipédii a doplňte do článku citácie, odkazy na spoľahlivé zdroje. |
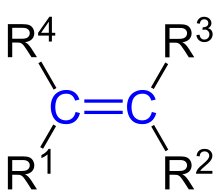
Alkény sú nenasýtené uhľovodíky s dvojitou väzbou v reťazci. uhlíka spojené dvojitou väzbou majú sp2 hybridizáciu.
Názvy
Alkény sa nazývajú aj alkylény alebo olefíny alebo olefinické uhľovodíky. Triviálny názov olefín pochádza z francúzštiny, pretože reakciou eténu s brómom vzniká olejovitý dibromid, ktorý nazvali gas olefaint, teda v preklade olejotvorný plyn.
Dvojitá väzba a jej charakteristika
Väzby, ktoré vychádzajú z atómov uhlíka v hybridizácii sp2, majú väzbový uhol 120° (2/3 π rad), preto ležia v jednej rovine. Dvojitá väzba bráni voľnej rotácii, čo umožňuje vznik stereoizomérov. Na uhlíkovom reťazci alkénov, kde sú jednoduché väzby medzi atómami uhlíka, vzniká štruktúrna izoméria. Prekrytie orbitálov p vo väzbe pí je menšie, preto aj jej energia je nižšia než u sigma väzby. Dvojitá väzba C=C je kratšia (134 pm) ako jednoduchá väzba C-C (154 pm), preto je aj pevnejšia. Dvojitá väzba sa u alkénov skladá z jednej pí a jednej sigma kovalentnej väzby.
Názvoslovie
Systémové názvy alkénov sú odvodené z alkánov výmenou prípony -án za -én. Pri alkénoch existuje izoméria polohy násobnej väzby, preto sa jej poloha označuje lokantom pred príponou -én a počet dvojitých väzieb charakteristickou predponou podobne ako u alkínov. Tieto predpony sú uvedené nižšie:
| Počet | Predpona |
|---|---|
| 1 | mono |
| 2 | di |
| 3 | tri |
| 4 | tetra |
| 5 | penta |
| 6 | hexa |
| 7 | hepta |
| 8 | okta |
| 9 | nona |
| 10 | deka |
| 11 | undeka |
| 12 | dodeka |
| 20 | ikoza |
| 30 | triakonta |
| 100 | hekta |
| 200 | dikta |
| 1000 | kilia |
| 2000 | dilia |
Homologický rad a všeobecné vzorce
Homologický rad závisí od všeobecného vzorca pre daný alkén. Všeobecné vzorce sú uvedené nižšie.
| Počet dvojitých väzieb | Vzorec |
|---|---|
| 1 | CnH2n |
| 2 | CnH2n-2 |
| 3 | CnH2n-4 |
| 4 | CnH2n-6 |
| 5 | CnH2n-8 |
Zástupcovia
Etén (etylén) je ľahký bezfarebný plyn sladkastej vône. Je horľavý a v určitom pomere so vzduchom výbušný. Získava sa pri chemickom spracovaní niektorých frakcií ropy. Patrí medzi najvýznamnejšie suroviny v modernej technológii. Vyrába sa z neho napríklad polyetylén (PE), etanol (C2H5OH), vinylchlorid (CH2=CHCl), rozpúšťadlá s Cl a v jeho prítomnosti rýchlo dozrieva ovocie (funguje ako hormón dozrievania).
Propén (propylén) je plynná látka, ktorá sa, podobne ako etén, vyrába z ropy. Používa sa hlavne na výrobu polypropylénu (PP), acetónu (CH3-CO-CH3), kuménu a ďalších organických látok.
Klasifikácia
Alkény s viacerými dvojitými väzbami sa skrátene nazývajú diény, triény, ..., polyény. Podľa toho, ako sú viaceré dvojité väzby v reťazci usporiadané, sa delia na:
- Kumulované - 2-ité väzby vychadzajú z 1 uhlíka.
- Konjugované - medzi každými dvoma 2-itými väzbami je 1 jednoduchá väzba.
- izolované - medzi 2-tými väzbami sú najmenej 2 jednoduché väzby.
Vznik a príprava
- CH3-CH2-CHX-CH3 → CH3-CH=CH-CH3 + HX
- z 1,2-dihalogénuhľovodíkov elimináciou:
- CH3-CHX-CHX-CH3 → CH3-CH=CH-CH3 + X2
- CH3-CH2-CHOH-CH3 → CH3-CH=CH-CH3 + H2O
- CH3-CH2-CH2-CH3 → CH3-CH=CH-CH3 + H2
Reakcie
- Adícia
- elektrofilná - potrebné elektrofilné činidlo
- radikálová - prebieha za vzniku radikálov
- cis adícia (označovaná aj ako Z-adícia) - pri vzniknutých derivátoch charakteristické skupiny ležia v 1 rovine
- Oxoreakcia - reakcia s CO, H2O, H2
- Polymerizácia -vznikajú polyméry, teda plasty
- Substitúcia - dochádza k nahradzovaniou vodíka charakteristickou skupinou
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antropológia
Aplikované vedy
Bibliometria
Dejiny vedy
Encyklopédie
Filozofia vedy
Forenzné vedy
Humanitné vedy
Knižničná veda
Kryogenika
Kryptológia
Kulturológia
Literárna veda
Medzidisciplinárne oblasti
Metódy kvantitatívnej analýzy
Metavedy
Metodika
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk
